Elizabeth Davlantes, MD1; Jaume Jorba, PhD2; Elizabeth Henderson2; Kelly Bullard, MS2; Signe. A. Deka, PhD3; Anfumbom Kfutwah, PhD4; Javier Martin, PhD5; Maël Bessaud, PhD6; Lester M. Shulman, Ph.D.7; Kaija Hawes, MBA8; Ousmane M. Diop, PhD9; Ananda S.Bandyopadhyay, MBBS8; Simona Zipursky, M.Sc.9; Cara C. Burns, Ph.D.2 (Voir l’affiliation de l’auteur)
Altmétriques :
Citation:
Apparence:
L’affichage est le même que celui de la page vue plus le téléchargement du PDF
Des flambées de poliovirus circulant dérivé d’une souche vaccinale (PVDVc) peuvent survenir lorsque les souches du vaccin antipoliomyélitique oral (le plus souvent, le vaccin antipoliomyélitique oral monovalent Sabin de type 2) [mOPV2]) subit une circulation prolongée dans des populations sous-vaccinées, entraînant une réversion génétique vers la neurovirulence. Un nouveau vaccin oral contre le poliovirus de type 2 (nVPO2) a été développé. Des essais cliniques ont montré qu’il était moins susceptible que le VPOm2 de revenir à des variantes paralysantes et qu’il présentait des modifications génétiques limitées pour une utilisation initiale sur le terrain (1–4). Environ 700 millions de doses de nVPO2 ont été administrées dans le monde en réponse à l’épidémie de PVDVc de type 2 (PVDVc2). Les détections de PVDVc2 provenant de l’utilisation du nVPO2 depuis son lancement initial entre mars 2021 et le 7 septembre 2023 sont décrites dans ce rapport.
Enquête et résultats
La surveillance de la poliomyélite et les données de laboratoire recueillies dans le cadre de l’Initiative mondiale pour l’éradication de la poliomyélite sont examinées. Entre août 2021 et juillet 2023, sept occurrences de PVDVc2 d’origine nVPO2 provenant de 61 cas de paralysie et de 39 échantillons de surveillance environnementale (déchets) ont été détectées dans six pays, tous en Afrique : Burundi, République centrafricaine (RCA), République démocratique du Congo. (Congo), le Nigéria, la Tanzanie et la Zambie (Nombre). L’isolat présentait des différences limitées par rapport à sa souche vaccinale nOPV2 parent dans la région codante pour la protéine de capside VP1 (six à 16 substitutions de nucléotides), ce qui indique que la surveillance a détecté son émergence relativement tôt après la vaccination. Cette activité a été examinée par le CDC, considérée comme n’étant pas de la recherche, et a été menée conformément à la loi fédérale et aux politiques applicables du CDC.*
Quatre des sept cas de PVDVc2 en circulation provenant de l’utilisation du nVPO2 ont été détectés uniquement dans les régions infranationales de leur pays d’origine (RCA, RDC et Nigeria), deux se sont propagés à d’autres régions du pays d’origine (RCA et RDC), et l’une s’est propagée du pays d’origine (RDC) aux pays voisins (Burundi, Tanzanie et Zambie). Trois foyers se propageant à l’intérieur ou à l’extérieur du pays d’origine (tous originaires du Congo) pourraient être en cours, la dernière détection remontant à juillet 2023. L’émergence la plus importante et la plus répandue, le RDC-SKV-1, a été détectée pour la première fois dans la province du Sud-Kivu, en RDC. en 2024. septembre 2022 ; Des virus issus de cette émergence ont été identifiés dans six provinces du Congo et dans les pays voisins du Burundi, de la Tanzanie et de la Zambie. RDC-SKV-1 a été détecté en juillet 2023 en Tanzanie.
Conclusions et premières actions
Le potentiel de mutation et de réversion de la neurovirulence est un risque rare mais connu avec tous les vaccins antipoliomyélitiques oraux vivants atténués ; L’utilisation intensive du nVPO2 dans le monde depuis mars 2021 suggère que la guérison se produit moins fréquemment qu’avec le VPOm2 (4). Les estimations préliminaires suggèrent que l’émergence du PVDVc2 se produit après l’utilisation du VPOm2 à raison d’une occurrence pour 10 millions de doses de VPOm2 administrées ; pour le nVPO2, ce chiffre est environ 10 fois inférieur, soit une occurrence pour 100 millions de doses. Comme c’est le cas pour toutes les émergences de PVDVc, les flambées de PVDVc2 dérivées du nVPO2 sont plus susceptibles de survenir lorsque les activités de vaccination adjuvante (AIS) avec le nVPO2 n’atteignent pas une couverture élevée dans les populations faiblement immunisées contre le poliovirus (5). Pour lutter contre toutes les épidémies de PVDVc2 et réduire leur apparition à l’avenir, une réponse rapide aux AVS atteignant tous les enfants ciblés est essentielle.
Note de remerciement
l’Institut national des maladies infectieuses d’Afrique du Sud ; Institut Pasteur de Bangui, République Centrafricaine ; Institut Pasteur, France ; Institut national de recherche biomédicale, République démocratique du Congo ; Feyrouz Kurji.
1Division de la vaccination mondiale, Centre pour la santé mondiale, CDC ; 2Division des maladies virales, Centre national de vaccination et des maladies respiratoires, CDC ; 3Programme de recherche, d’analyse et de services géospatiaux, Agence pour le registre des substances toxiques et des maladies, Atlanta, Géorgie ; 4Réseau régional de laboratoires de polio, Bureau régional de l’Organisation mondiale de la Santé pour l’Afrique, Brazzaville, République du Congo ; 5Division de l’Agence de réglementation des vaccins, des médicaments et des produits de santé, Potters Bar, Royaume-Uni ; 6Institut Pasteur, Université Paris Cité, Unité de Détection et Signalisation des Virus, Paris, France ; 7Laboratoire central de virologie, Service de santé publique, ministère israélien de la Santé, Tel Aviv, Israël ; 8Fondation Bill & Melinda Gates, équipe Polio, Seattle, Washington ; 9Organisation mondiale de la santé, Genève, Suisse.
Référence
- Ouais MT, Bujaki E, Dolan PT et al. Mise au point d’un vaccin vivant atténué contre la polio pour empêcher le retour de la virulence. Microbe hôte cellulaire 2020 ; 27 : 736–751.e8. https://doi.org/10.1016/j.chom.2020.04.003 PMID:32330425
- Martin J, Burns CC, Jorba J et al. Caractérisation génétique d’un nouveau virus du vaccin antipoliomyélitique oral de type 2 pendant la phase d’utilisation initiale dans la liste d’utilisation d’urgence – dans le monde entier, de mars à octobre 2021. MMWR Morb Mortal Wkly Rep 2022 ; 71 : 786–90. https://doi.org/10.15585/mmwr.mm7124a2 PMID:35709073
- Zaman K, Bandyopadhyay AS, Hoque M et al. Évaluation de l’innocuité, de l’immunogénicité et de la clairance fécale du vaccin oral contre la polio de type 2 chez les nouveau-nés en bonne santé au Bangladesh : un essai clinique randomisé et contrôlé de phase 2. Lancet 2023 ; 401 : 131–9. https://doi.org/10.1016/S0140-6736(22)02397-2 PMID:36495882
- Bandyopadhyay AS, Zipursky S. Nouveaux outils pour éradiquer un fléau ancien : une nouvelle histoire sur le vaccin oral contre la polio de type 2. Lancet Infect Dis 2023;23 :e67-71. https://doi.org/10.1016/S1473-3099(22)00582-5 PMID:36162417
- Pons-Salort M, Burns CC, Lyons H et al. Empêche l’émergence de poliovirus dérivés d’une souche vaccinale pendant la fin de la polio. PLoS Pathog 2016;12 :e1005728. https://doi.org/10.1371/journal.ppat.1005728 PMID:27384947
 NOMBRE. Détection du poliovirus de type 2 circulant dérivé d’une souche vaccinale associée à l’utilisation d’un nouveau vaccin oral contre le poliovirus de type 2, par cohorte d’émergence – Afrique, 2021-2023
NOMBRE. Détection du poliovirus de type 2 circulant dérivé d’une souche vaccinale associée à l’utilisation d’un nouveau vaccin oral contre le poliovirus de type 2, par cohorte d’émergence – Afrique, 2021-2023
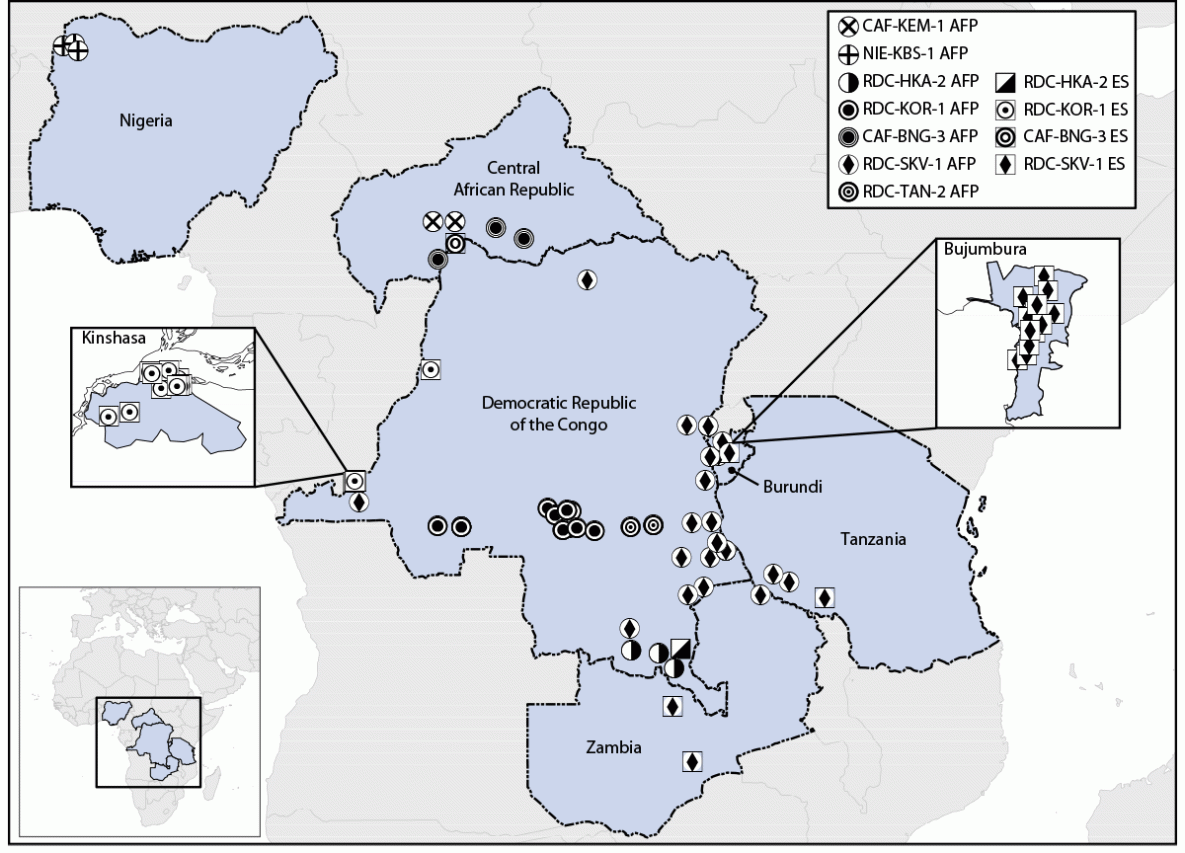
Abréviation: AFP = cas de paralysie flasque aiguë ; ES = isolement de surveillance environnementale.
Citation suggérée pour cet article : Davlantes E, Jorba J, Henderson E et al. Notes du terrain: Émergence du virus de la polio de type 2 dérivé des vaccins en circulation liée à l’utilisation d’un nouveau vaccin oral contre le virus de la polio de type 2 — Six pays africains, 2021-2023. MMWR Morb Mortal Wkly Rep 2023 ; 72 : 1041-1042. EST CE QUE JE: http://dx.doi.org/10.15585/mmwr.mm7238a4.
MMWR Et Rapport hebdomadaire sur la morbidité et la mortalité est une marque de service du ministère américain de la Santé et des Services sociaux.
L’utilisation de noms commerciaux et de sources commerciales est uniquement destinée à l’identification et n’implique pas l’approbation du ministère américain de la Santé et des Services sociaux.
Les références à des sites Internet non-CDC sont fournies à titre de service à MMWR lecteurs et ne constitue ni n’implique l’approbation de ces organisations ou de leurs programmes par le CDC ou le ministère américain de la Santé et des Services sociaux. CDC n’est pas responsable du contenu des pages trouvées sur ces sites. L’adresse URL est répertoriée dans MMWR à jour à la date de publication.
Toutes les versions HTML de MMWR les articles sont produits à partir d’épreuves finales grâce à un processus automatique. Cette conversion peut entraîner des erreurs de traduction de caractères ou de format dans la version HTML. Les utilisateurs sont renvoyés à la version électronique PDF (https://www.cdc.gov/mmwr) et/ou à la version originale MMWR copies papier pour les versions imprimables des textes, figures et tableaux officiels.
Les questions ou les messages concernant les erreurs de formatage doivent être adressés à mmwrq@cdc.gov.







